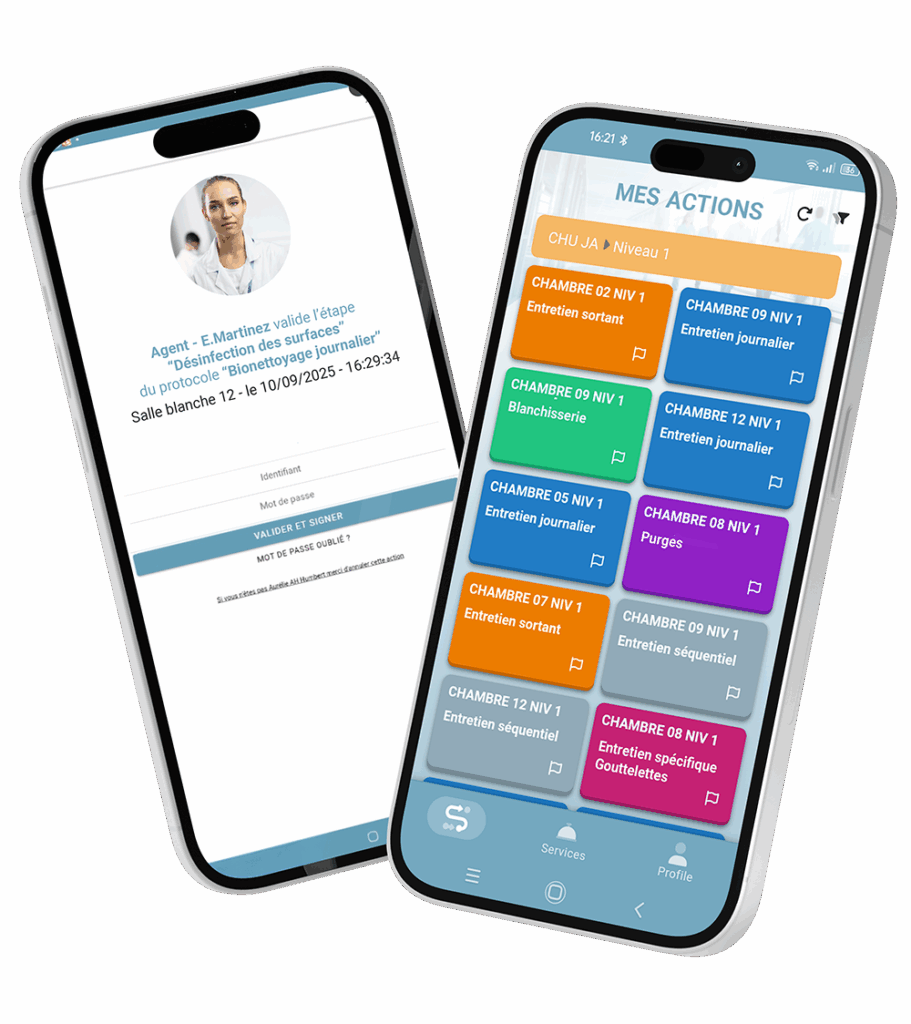
Que ce soit dans l’industrie pharmaceutique, la santé ou les laboratoires, les procédés d’hygiène et de désinfection sont régis par des normes sécuritaires inflexibles. Le non-respect de ces réglementations peut avoir des conséquences désastreuses, autant sur la qualité des produits commercialisés que sur la vie des populations. Intoxications, morts dues à des syndromes bactériologiques ou encore présence de matières toxiques ont fait la une des journaux en 2025. L’ultra-propreté impose la traçabilité des interventions et pour cela faire appel à des outils conformes aux normes en vigueur est indispensable. Et pour rester en conformité, la norme 21 CFR part 11 est obligatoire. Vous souhaitez prétendre à des certifications ISO ou d’ultra-propreté ? Découvrez nos conseils pour instaurer une traçabilité conforme à la norme 21 CFR part 11.

Qu'est-ce que la norme CFR 21 part 11 ?
Créée en 1997 par l’organisation américaine Food & Drug Administration (FDA), la norme 21 CFR part 11 encadre avec fermeté les enregistrements et les signatures électroniques réalisées à chaque étape d’un ou plusieurs protocoles d’ultra-propreté. Cette réglementation définit les caractéristiques de création, de validation, de stockage et de protection des signatures, afin que celles-ci soient considérées comme des preuves tangibles de réalisation d’un protocole.
Dans les environnements critiques et les zones exigeantes, l’ultra-propreté est mesurée selon plusieurs paramètres. Qualité de l’air, concentration
des particules, hygrométrie, respect des points de passage et des sas d’habillages… Tous ces indicateurs doivent être impérativement comptabilisés, tracés, répertoriés et horodatés pour un suivi méthodique de la conformité des procédures. La norme 21 CFR part 11 établit un référentiel de critères de sécurité à respecter pour assurer cette intégrité et éviter les erreurs ou pertes d’informations.
Les critères à respecter
Entre autres, la norme 21 CFR part 11 impose le respect des éléments suivants :
- Identification de la personne qui a saisi ou modifié les données via une politique de mots de passe très poussée ou une double authentification
- Date, horodatage et signature électronique formelle pour chaque action réalisée
- Intégration de cette signature dans un audit trail intouchable
- Protection des données contre toute modification non autorisée
- Historique infalsifiable des actions et des validations
La mise en place de ces systèmes de vérification doit en amont être explicitement présentée aux utilisateurs ou aux agents de production. Dans l’Union européenne, leur consentement est obligatoire pour respecter la RGPD.
Pourquoi être conforme à la norme 21 CFR part 11 ?
Peu importe votre domaine d’activité, la norme 21 CFR part 11 atteste de la fiabilité de vos parcours d’interventions et de vos contrôles qualité. Selon les pays et les zones d’exportation, comme par exemple aux États-Unis, cette norme est obligatoire pour la commercialisation de produits pharmaceutiques, biomédicaux ou biotechnologiques. L’obligation est même élargie à vos prestataires de services et fournisseurs, si ces derniers sont directement impliqués dans votre chaîne de production (ultra-propreté, nettoyage, maintenance…).
Outre l’aspect réglementaire obligatoire, la norme 21 CFR part 11 permet aussi de rassurer vos clients et vos investisseurs. Elle garantit la sécurité et la traçabilité des données critiques en toutes circonstances grâce à des technologies de chiffrement et de cryptage avancées. En cas d’incident, cet historique vous permet d’accéder à un audit trail inviolable et de remonter rapidement à l’origine d’un dysfonctionnement. Cette visibilité sur les événements favorise la résolution rapide des anomalies. Les risques d’interruption de service sont donc minimisés et vos clients d’autant plus sereins.
Comment se conformer à la norme 21 CFR part 11 ?
Les auditeurs des certifications obligeant le respect de la norme 21 CFR part 11 s’appuient sur un certain nombre de livrables pour valider leur inspection. L’entreprise candidate doit fournir les pièces justificatives suivantes :
- La mise en place des procédures « Computer System Validation » qui démontrent la traçabilité, la qualification et l’évolution des interactions dans l’ensemble des systèmes informatisés ou des outils de gestion documentaire.
- Le déploiement de contrôles d’accès sur toutes les étapes de production ou les protocoles qui y sont rattachés d’une manière ou d’une autre.
- La mise en place d’un système de blocage en cas d’erreurs consécutives sur une étape de validation ou d’une tentative quelconque de fraude
- La disponibilité d’un audit trail inviolable, composé de preuves opposables répertoriées
- La formation, voire le passage d’habilitations spécifiques, des équipes aux nouvelles procédures sécuritaires de la 21 CFR Part 11
Comment réussir ses audits de certification ?
Pour valider votre évaluation, le mot d’ordre est la préparation ! Un audit réfléchi et structuré correctement vous assurera une validation de la certification recherchée et la conformité à la norme 21 CFR part 11 à coups sûrs. Avant, pendant et après : voici tous nos conseils pour réussir vos évaluations.
Faites un état des lieux de votre niveau actuel
Le premier point décisif est de tout d’abord faire une auto-évaluation complète de votre entreprise. Pour ce faire, vous devez scruter au peigne fin vos processus opérationnels, vos structures décisionnelles et les différents échanges entre les parties prenantes :
- Définir le périmètre de l’audit : Avant toute chose, lister intégralement tous les systèmes ou les parcours potentiellement concernés par l’évaluation.
- Analyser le parcours opérationnel : Comment sont tracées et validées les étapes de production ? Qui est habilité pour effectuer ces validations ? Où sont stockées les données ? Y’a-t-il des outils déjà mis en place ? Quelles sont les contraintes du système informatique ? Vous devez vérifier que chaque étape de la chaîne, de la réception des échantillons jusqu’à la commercialisation, est bien conforme aux demandes de la norme 21 CFR part 11. Dans le cas contraire, vous aurez un aperçu concret des étapes à finaliser pour obtenir votre certification. Si une partie de vos processus repose encore sur des fichiers Excel ou un ERP non sécurisé, cela constitue une non-conformité majeure au regard de la norme 21 CFR Part 11.
- Collecter la documentation et lister les exigences réglementaires applicables en fonction du type de support et de sa vocation. Comparer les pré-requis avec la réalité terrain et répertorier les points à développer pour l’obtention de la certification.
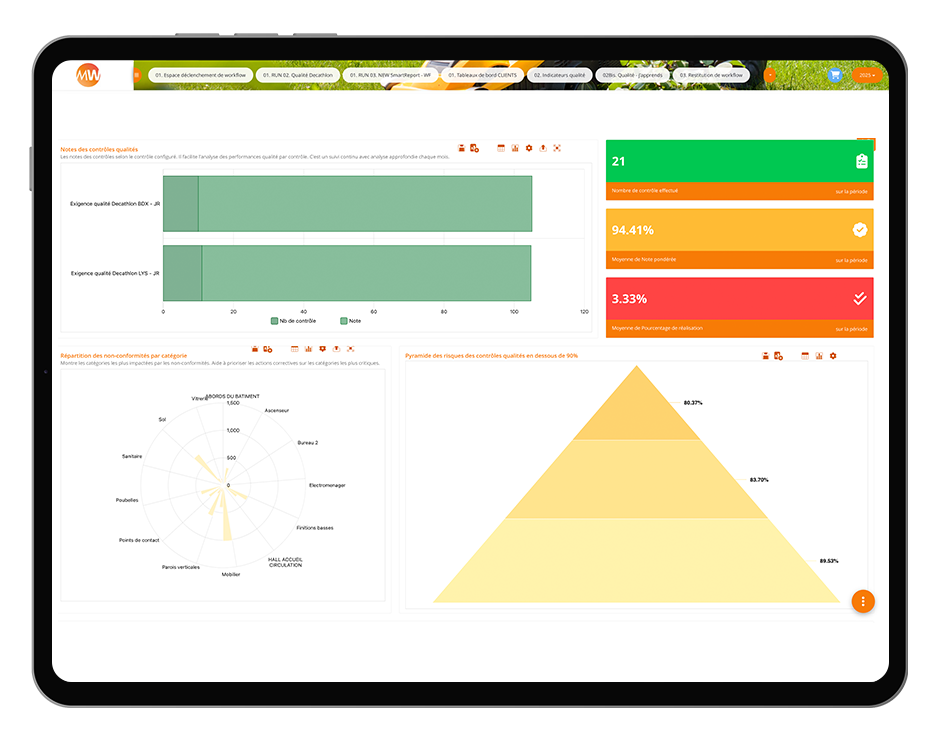
Mise en place des protocoles documentés
Forcément, après la théorie vient la pratique ! Pour respecter la conformité à la norme 21 CFR part 11, vous devez numériser consciencieusement vos parcours d’intervention pour qu’ils se calquent dans la grille de référence. Et comment faire ? En digitalisant la traçabilité avec des outils digitaux performants et adaptés. Rien ne sert de passer des heures à essayer de concevoir des solutions en interne, gagnez du temps et appelez des experts en la matière !
Choisir des outils “prêts à l’emploi” ou “conformes 21 CFR part 11” vous évitera bien de mauvaises surprises. Un fournisseur expérimenté pourra vous orienter dans votre projet et détectera en quelques minutes les risques de non-conformité. Voici les éléments à ne pas négliger dans le choix de votre partenaire technologique :
- Vérifiez que le dispositif de signatures électroniques fourni est bien conforme à la norme 21 CFR part 11 et exigez la documentation relative à cette distinction.
- Assurez-vous que l’outil s’intègre avec votre environnement existant (réseau, sécurité, sauvegardes, authentification centralisée…).
- Vérifiez la pérennité du fournisseur et l’évolutivité de la solution : migrations, mises à jour du logiciel, support technique…
- Contrôler que la formation et l’accompagnement à la prise en main sont bien incluses dans le coût d’acquisition et de déploiement.
Les meilleurs outils pour être conforme à la norme 21 CFR part 11
- La plateforme de traçabilité des interventions MoveWORK Flow et son application terrain myMissions Indoor
Le logiciel de gestion qualité MasterControl
Le logiciel de gestion de laboratoire LabWare
Vérification et ajustement avant l'audit 21 CFR part 11
L’ultime étape avant de demander une date pour votre audit est le déploiement d’une phase de tests et d’examen du système déployé. Les signatures électroniques sont bien remontées automatiquement ? Les audits trails sont-ils bien verrouillés ? Les chiffrements CSV sont-ils conformes aux formats pré-requis ? Un à un, vous devez vérifier que les contrôles fonctionnent comme prévu :
- Contrôles d’accès et d’authentification
- Signatures électroniques et liens avec les enregistrements
- Mode de récupération des mots de passe
- Traçabilité des modifications (versionning, changement, suppression…)
- Sécurité des données, sauvegardes, intégrité
- Déclenchement des journaux d’événements
- Révision périodique des logs
Formation et habilitations des équipes
Comme expliqué précédemment, les intervenants d’ultra-propreté ou des environnements critiques doivent tous acquérir des compétences spécifiques pour garantir la sécurité sanitaire. Agents d’entretien, contrôleurs qualité, responsables de sites, directeurs d’établissement… Tous ont l’obligation d’être habilités selon leur secteur d’activité pour pouvoir prétendre à des certifications exigeant la conformité à la norme 21 CFR part 11.
D’un côté, l’employeur doit passer plusieurs évaluations, qui engageront ensuite sa responsabilité
dans la chaîne de production. Ses habilitations dépendent de l’industrie (agroalimentaire, pharmaceutique, santé, microélectronique…) et couvriront l’ensemble des employés sous sa tutelle. De l’autre, les opérationnels doivent également passer des formations précises relatives aux normes 21 CFR part 11, aux engagements pris et à l’utilisation des outils digitaux qui en découlent.
Mais, attention ! Il ne suffit pas que vos agents soient formés sur le papier pour que votre entreprise réponde à la norme 21 CFR part 11. Avant un éventuel audit, interroger les utilisateurs pour confirmer que les pratiques réelles correspondent aux procédures décrites théoriquement. Les auditeurs peuvent très bien questionner votre personnel au cours de l’évaluation.
Réaliser un audit blanc
Vous voulez vraiment mettre toutes les chances de votre côté ? Alors, prenez la place des auditeurs et rédigez un rapport présentant :
- Les constatations positives et négatives sur votre parcours opérationnel : écarts, non-conformités, oublis…
- Les risques associés
- Les actions correctives à mettre en place avec priorités et échéances
Vous n’avez aucun point à revoir ? Parfait, vous êtes prêts à être audités pour des certifications nécessitant la norme 21 CFR part 11 ! Au contraire, il y a encore des lacunes dans la traçabilité ? Alors recommencez tout le processus de vérification depuis le début, en ajustant bien sûr les éléments non conformes.